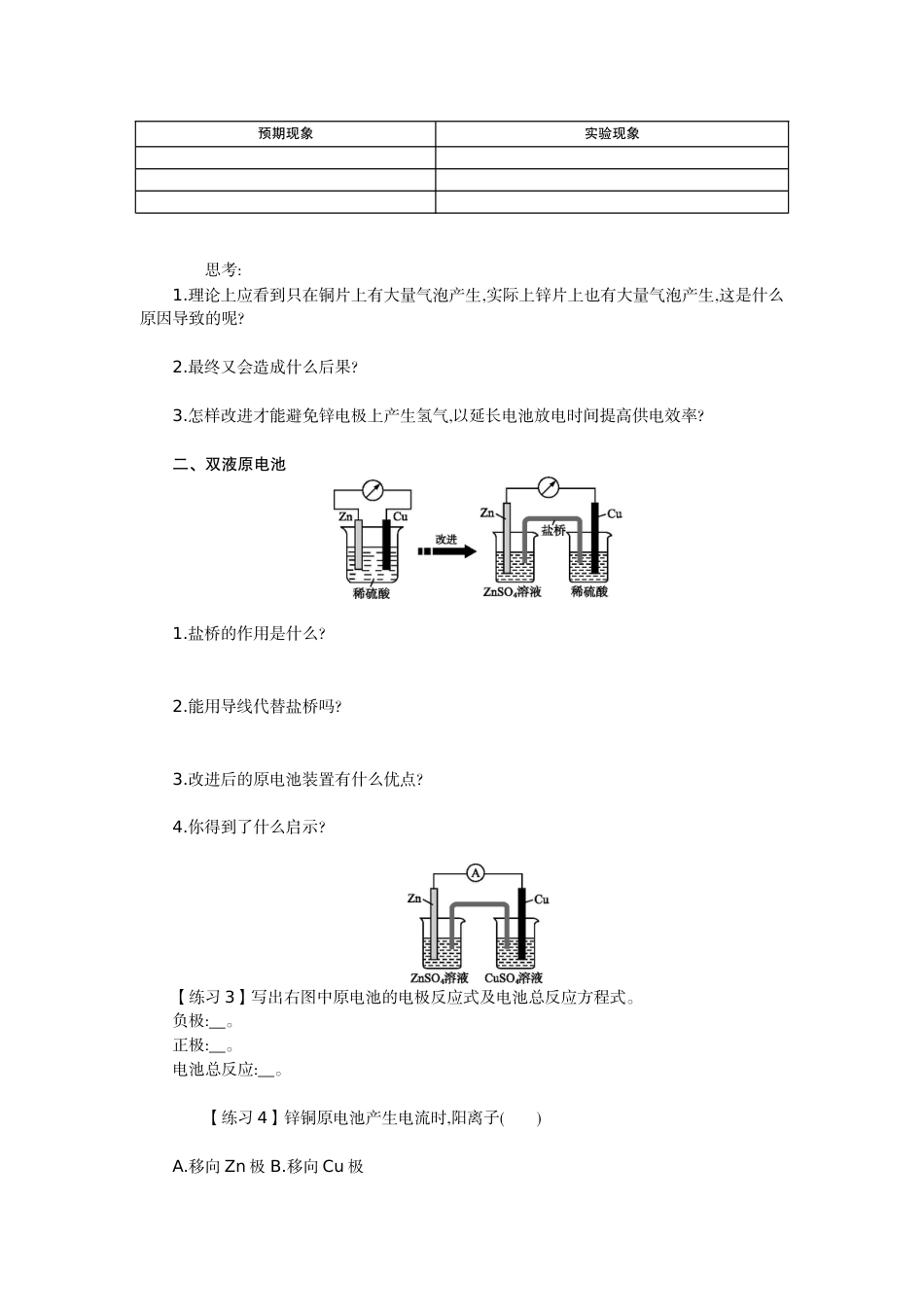
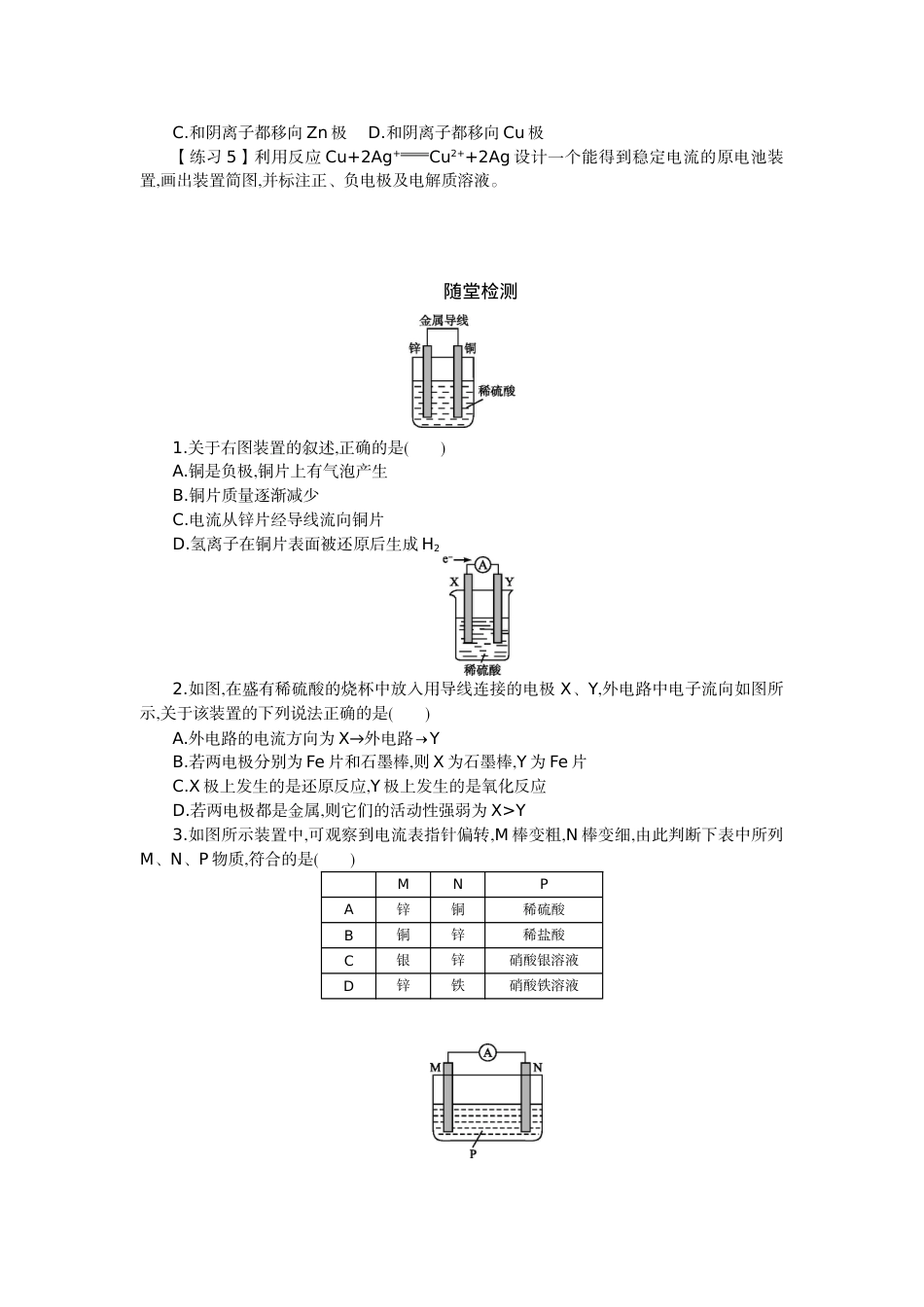
第四章电化学基础第一节原电池学习目标1.了解双液原电池的工作原理及构成条件;2.能正确书写原电池的电极反应式和电池总反应方程式;3.掌握盐桥的作用及工作原理。复习回顾1.氧化还原反应的本质是什么?2.将锌片放入CuSO4溶液,在反应过程中转移的电子能否形成电流?为什么?3.怎样才能使在氧化还原反应过程中转移的电子形成电流呢?课堂探究一、原电池1.定义:。2.构成条件:。3.电极的判断:。【练习1】判断以下装置能否构成原电池,若能构成,请指出原电池的正、负极。【练习2】下面哪个反应能够设计成原电池?HCl(aq)+NaOH(aq)NaCl(aq)+H2O(l)ΔH<0CO(g)+H2O(g)CO2(g)+H2O(g)ΔH>0Zn(s)+H2SO4(aq)ZnSO4(aq)+H2(g)ΔH<0请你利用下列反应原理设计合理的原电池装置,并完成下表:【实验探究】Zn(s)+H2SO4(aq)ZnSO4(aq)+H2(g)ΔH<0预期现象实验现象思考:1.理论上应看到只在铜片上有大量气泡产生,实际上锌片上也有大量气泡产生,这是什么原因导致的呢?2.最终又会造成什么后果?3.怎样改进才能避免锌电极上产生氢气,以延长电池放电时间提高供电效率?二、双液原电池1.盐桥的作用是什么?2.能用导线代替盐桥吗?3.改进后的原电池装置有什么优点?4.你得到了什么启示?【练习3】写出右图中原电池的电极反应式及电池总反应方程式。负极:。正极:。电池总反应:。【练习4】锌铜原电池产生电流时,阳离子()A.移向Zn极B.移向Cu极C.和阴离子都移向Zn极D.和阴离子都移向Cu极【练习5】利用反应Cu+2Ag+Cu2++2Ag设计一个能得到稳定电流的原电池装置,画出装置简图,并标注正、负电极及电解质溶液。随堂检测1.关于右图装置的叙述,正确的是()A.铜是负极,铜片上有气泡产生B.铜片质量逐渐减少C.电流从锌片经导线流向铜片D.氢离子在铜片表面被还原后生成H22.如图,在盛有稀硫酸的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示,关于该装置的下列说法正确的是()A.外电路的电流方向为X→外电路→YB.若两电极分别为Fe片和石墨棒,则X为石墨棒,Y为Fe片C.X极上发生的是还原反应,Y极上发生的是氧化反应D.若两电极都是金属,则它们的活动性强弱为X>Y3.如图所示装置中,可观察到电流表指针偏转,M棒变粗,N棒变细,由此判断下表中所列M、N、P物质,符合的是()MNPA锌铜稀硫酸B铜锌稀盐酸C银锌硝酸银溶液D锌铁硝酸铁溶液4.按下图装置进行实验,若x轴表示流出负极的电子的物质的量,则y轴可表示()①c(Ag+)②c(N)③a棒的质量④b棒的质量⑤溶液的质量A.①③B.③④C.①②④D.②5.对于原电池的电极名称,叙述错误的是()A.发生氧化反应的一极为负极B.正极为电子流入的一极C.比较不活泼的金属为负极D.电流流出的一极为正极6.在如图所示的装置中,a的金属活动性比氢要强,b为石墨棒,下列关于此装置的叙述不正确的是()A.石墨棒上有气体放出,溶液pH变大B.a是正极,b是负极C.导线中有电子流动,电子从a极经导线流向b极D.a极上发生了氧化反应7.如图所示,烧杯内盛有浓硝酸,在烧杯中放入用铜线相连的铁、铅两个电极,构成原电池。已知原电池停止工作时,Fe、Pb都有剩余。下列有关说法正确的是()A.Fe比Pb活泼,始终作负极B.Fe在浓硝酸中钝化,始终不会溶解C.电池停止工作时,烧杯中生成了Fe(NO3)3D.利用浓硝酸作电解质溶液不符合“绿色化学”思想8.原电池的电极名称不仅与电极材料的性质有关,也与电解质溶液有关。下列说法中不正确的是()A.由Al、Cu、稀硫酸组成原电池,其负极反应为Al-3e-Al3+B.由Mg、Al、NaOH溶液组成原电池,其负极反应式为Al-3e-+4OH-Al+2H2OC.由Fe、Cu、FeCl3溶液组成原电池,其负极反应式为Cu-2e-Cu2+D.由Al、Cu、浓硝酸组成原电池,其负极反应式为Cu-2e-Cu2+9.锌铜原电池(如图)工作时,下列叙述正确的是()A.正极反应为Zn-2e-Zn2+B.电池总反应为Zn+Cu2+Zn2++CuC.在外电路中,电流从负极流向正极D.盐桥中的K+移向ZnSO4溶液10.锂电池是一代新型高能电池,它以质量轻、能量高而受到了普遍重视,目前已研制成功多种锂电池。某种锂电池的总反应方程式为Li+MnO2LiMnO2,下列说法正确的是()A.Li是正极,电极反应为Li-e-Li+B.Li是负极,电极反应为Li-e-Li+C.MnO2是负极,电极反应为MnO2+e-MnD.Li是负极,电极反应为Li-2e-Li2+参考答案复习回顾1.氧化还原反应的本质是...